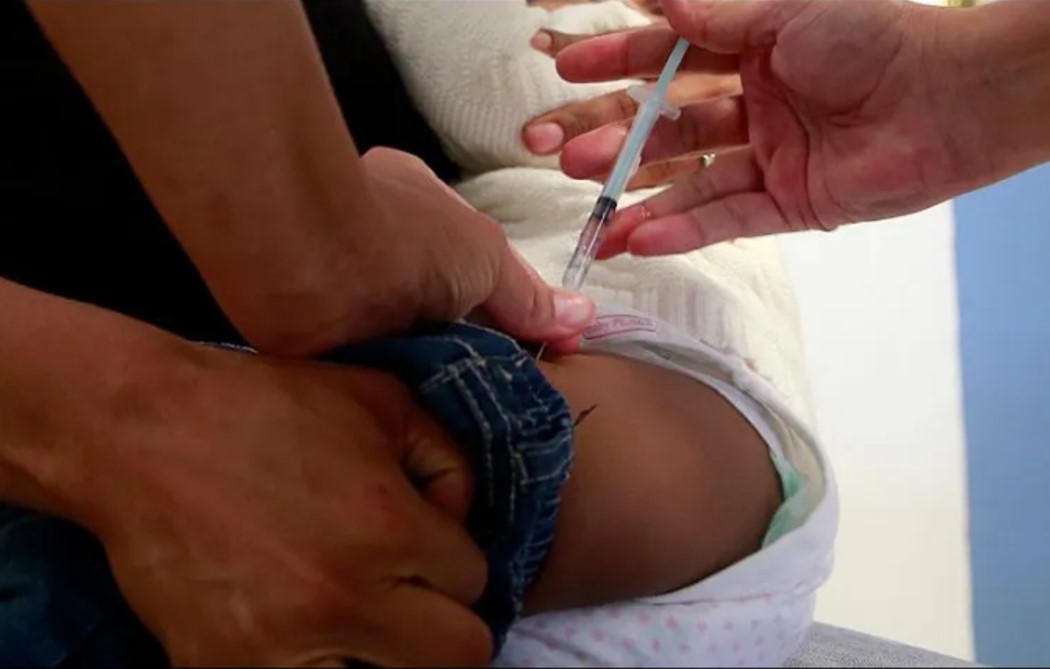
Las farmacéuticas Pfizer y BioNTech aseguraron lunes que “tres dosis” de su vacuna contra COVID ofrecen “una respuesta inmune fuerte, una alta eficacia y una seguridad favorable” en niños entre 6 meses y 5 años.
Las compañías destacaron en un comunicado que, de acuerdo con la información recabada en sus ensayos clínicos, las tres dosis cumplen con los criterios requeridos para una aprobación de emergencia por parte de las autoridades sanitarias.
La nota asegura que durante los ensayos se observó una eficacia del 80.3 % después de la tercera dosis en un momento en el que la variante ómicron de COVID era la predominante.
Asimismo, apunta que la tercera dosis de 3 microgramos fue bien tolerada por mil 678 niños menores de cinco años “con un perfil de seguridad similar al placebo”.
“La mayoría de los eventos adversos fueron leves o moderados”, asevera la nota.
“El nivel de dosis de 3 microgramos, las cuales representa una décima parte de la dosis para adultos, fue seleccionada para menores de 5 años en función de la seguridad, tolerabilidad e inmunogenicidad”, subrayan las farmacéuticas.
El director ejecutivo de Pfizer, Albert Bourla, aseguró que después de estos datos esperan completar su solicitud a los reguladores sanitarios de todo el mundo con el objetivo de que su vacuna sea aprobada para dicho rango de edad.
Moderna solicitó el pasado abril a las autoridades sanitarias estadounidenses y europeas la autorización de emergencia de su vacuna contra COVID para niños en edades entre los seis meses y los seis años, convirtiéndose en la primera compañía en pedir dicha aprobación para este rango de edad.